 De informatie in dit artikel is overgenomen uit een blogpost die onder CC-BY-licentie is gepubliceerd, Darren Smyth, IPKat.
De informatie in dit artikel is overgenomen uit een blogpost die onder CC-BY-licentie is gepubliceerd, Darren Smyth, IPKat.
In the list of Decisions, there have been a number of cases where substantial procedural violations have been found by the Board:
T 1880/11 – Failure to appoint Oral Proceedings on the subject of adaptation of the description after first appeal decision constituted a substantial procedural violation. Even though Oral Proceedings had already been held before the first refusal of the application (which had been successfully appealed), the applicant was entitled to a second Oral Proceedings on the subject of adaptation because the subject of the requested second Proceedings was different from the first.
T 0645/11 – Refusal of application after only one examination report is not always a substantial procedural violation, but was found to be so in this case. This is a salutary reminder to European Patent Attorneys to ALWAYS request Oral Proceedings, this being all too easily forgotten.
T 1285/11 – Refusal of an application having provided no reasoned statement as to why the arguments of the applicant had not been accepted was found to be a violation of Article 113(1) EPC (the right to be heard), and, accordingly, a substantial procedural violation. By coincidence, this case was a Pfizer application relating to polymorphs, similar to a case which was the subject of an earlier post.
Another substantial procedural violation was found in T 0382/10 – there seems to have been a misunderstanding between the representative of the applicant and the Examining Division during the Oral Proceedings, which resulted in a premature and unexpected refusal of the application.
On the other hand, in T 0698/11, the Board held that the Examining Division had been wrong to allege that a particular feature was "notorious knowledge" or indisputable common general knowledge, and that a further search should have been performed. However, this was considered to constitute an error of judgement on a substantive issue rather than an incorrect conduct of the procedure. Therefore, this was not considered to be a substantial procedural violation.
Turning now to other matters: In T 0418/07 the Respondent appointed two firms of representatives and requested the Board to send materials to both firms, which the Board declined to do. Furthermore, the Respondent announced before Oral Proceedings that it would use German at the Oral Proceedings and requested the Board to provide translation from German into English for the benefit of the Appellant and of one of its own employees who would attend the Oral Proceedings and who does not speak German. The Board pointed out that the translation available under Rule 4(1) was available for the benefit of the other party, not the party using the language that was not the language of the proceedings. In this case, the Appellant had indicated that he would not attend the Oral Proceedings, so the request for translation was refused.
T 0960/08 reminds us of the dangers that lurk when opponent status (or indeed the patent) is transferred around the time of the filing of an appeal. The Appeal was rejected as inadmissible because it was filed in the name of a party who the Board decided was not the correct opponent.
T 0065/11 is an example of the Boards of Appeal guarding their own jurisdiction. The case concerns re-establishment of the rights in respect of the time limit for filing the notice of appeal. The request for re-establishment was purportedly granted by a Formalities Officer for the Examining Division. The Board declared this null and void, pointing out that it was for the Board to decide on the re-establishment. But they proceeded to grant the request anyway.
T 0036/11 confirms that it is for the EPO, not the Patentee, to decide whether Opposition proceedings should continue if the Opponent withdraws their opposition. An appeal against a decision of the Opposition Division not to continue the proceedings in these circumstances was rejected as inadmissible on the basis that the Patentee was not adversely affected by the decision.
J 0018/10 reminds us to be very careful about withdrawing an application (which is usually done either to prevent publication or to obtain a refund of fees). If the applicant changes their mind, retraction of the withdrawal (that is, reinstatement of the application) is very difficult, and was not allowed in this case.
The EPO Boards of Appeal currently seem unable to decide whether double patenting is prohibited under the EPC (there being no explicit prohibition of double patenting in the text of the EPC), and, if so, what are the criteria for deciding what constitutes double patenting. T 1491/06 is the latest addition to the canon of cases, and had this to say:
In its decisions in cases G 1/05 and G 1/06 handed down on 28 June 2007 (OJ EPO 2008, 271 and 307, respectively) the Enlarged Board of Appeal held obiter (see point 13.4 of the identical Reasons):
"The Board accepts that the principle of prohibition of double patenting exists on the basis that an applicant has no legitimate interest in proceedings leading to the grant of a second patent for the same subject-matter if he already possesses one granted patent therefor." The board in decision T 1391/07 (not published in OJ EPO, point 2.6 of the Reasons), referring to the above decisions of the Enlarged Board, saw no basis for extending the existing practice to "cover claims not defining the same subject-matter but conferring... a scope of protection overlapping with each other only partially in the sense that some, but not all of the embodiments notionally encompassed by one of the claims would also be encompassed by the other one of the claims." The present board agrees with this view.
Applying this standard, the claims of the application in suit were held to be different from subject-matter of a patent already granted to the appellant, so there was no double patenting. Perhaps it is now time for this issue to be referred to the Enlarged Board of Appeal by the President of the EPO?
Finally, T 1336/09 reminds us that, while proceedings are still pending, the EPO will generally take into consideration third party observations, even if they are filed at a very late stage in the proceedings. Furthermore, it is perfectly permissible to file third party observations anonymously.
 Uitspraak ingezonden door Otto Swens, Vondst advocaten.
Uitspraak ingezonden door Otto Swens, Vondst advocaten.
 Over de vraag: Inbreuk op ABC voor werkzame stoffen alleen of in combinatie met andere werkzame stoffen? (exacte vraag, zie onder)
Over de vraag: Inbreuk op ABC voor werkzame stoffen alleen of in combinatie met andere werkzame stoffen? (exacte vraag, zie onder) Als randvermelding. Registratie van generieke geneesmiddelen. Wegens Europees gebruiksoctrooi heeft het CBG bepaald dat indicatie uit SPC en bijsluiter van generieke geneesmiddelen moet worden verwijderd en een standaardpassage in de bijsluiter daarvan moet worden opgenomen. De rechtbank is van oordeel dat de nationale bepalingen over de registratie van geneesmiddelen conform artikel 11 laatste alinea van Richtlijn 2004/27/EG kunnen worden uitgelegd, hetgeen verweerder dan ook terecht heeft gedaan. Argumenten tegen het opnemen van de standaardpassage in de bijsluiter van de generieke geneesmiddelen vinden geen steun in het recht en leiden niet tot vernietiging van het bestreden besluit. Het valt niet in te zien dat de standaardpassage in de bijsluiter uitnodigt tot gebruik, tot het voorschrijven of afleveren van het product noch uitnodigt tot octrooi-inbreuk.
Als randvermelding. Registratie van generieke geneesmiddelen. Wegens Europees gebruiksoctrooi heeft het CBG bepaald dat indicatie uit SPC en bijsluiter van generieke geneesmiddelen moet worden verwijderd en een standaardpassage in de bijsluiter daarvan moet worden opgenomen. De rechtbank is van oordeel dat de nationale bepalingen over de registratie van geneesmiddelen conform artikel 11 laatste alinea van Richtlijn 2004/27/EG kunnen worden uitgelegd, hetgeen verweerder dan ook terecht heeft gedaan. Argumenten tegen het opnemen van de standaardpassage in de bijsluiter van de generieke geneesmiddelen vinden geen steun in het recht en leiden niet tot vernietiging van het bestreden besluit. Het valt niet in te zien dat de standaardpassage in de bijsluiter uitnodigt tot gebruik, tot het voorschrijven of afleveren van het product noch uitnodigt tot octrooi-inbreuk. De informatie in dit artikel is overgenomen uit een blogpost die onder
De informatie in dit artikel is overgenomen uit een blogpost die onder  Bijdrage ingezonden door Jan Pieter Hustinx, Gertjan Kuipers en Tjibbe Douma,
Bijdrage ingezonden door Jan Pieter Hustinx, Gertjan Kuipers en Tjibbe Douma,  Overdracht octrooi(aanvragen). Internationale bevoegdheid van de rechter. Exclusieve bevoegdheid ex 80 ROW 1995 en 22 lid 4 EEX-Vo.
Overdracht octrooi(aanvragen). Internationale bevoegdheid van de rechter. Exclusieve bevoegdheid ex 80 ROW 1995 en 22 lid 4 EEX-Vo. Uitspraak ingezonden door Ruud van der Velden,
Uitspraak ingezonden door Ruud van der Velden,  In navolging van
In navolging van 
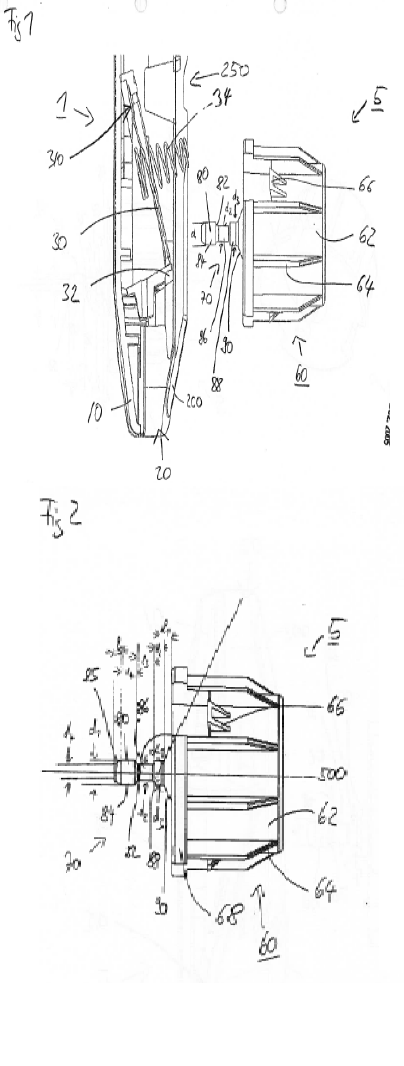 Octrooirecht. Voorrangsdocument. SCA legt zich toe op verzorgingsproducten, waaronder handdoekrollen. Zij is houdster van Europees octrooi
Octrooirecht. Voorrangsdocument. SCA legt zich toe op verzorgingsproducten, waaronder handdoekrollen. Zij is houdster van Europees octrooi 




















































































